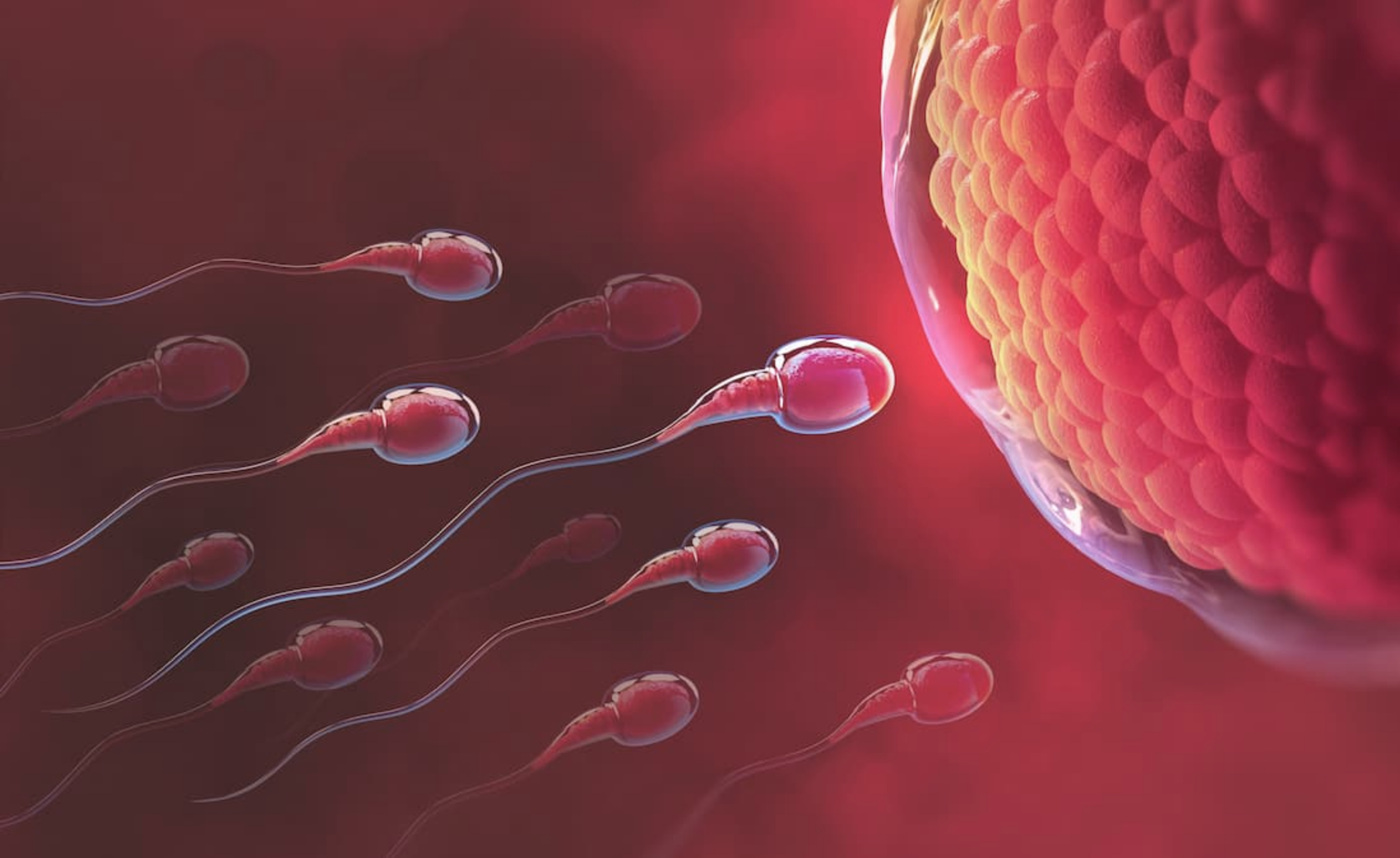
Un equipo de la Universidad de Salud y Ciencia de Oregón (OHSU), liderado por Shoukhrat Mitalipov, logró un avance histórico en la reproducción asistida: crear óvulos humanos funcionales a partir de células de la piel.
El estudio, publicado en Nature Communications, utiliza la técnica de Transferencia Nuclear de Células Somáticas (SCNT), la misma que permitió clonar a la oveja Dolly en 1996.
Más del 10% de los nacimientos en España provienen ya de tratamientos de reproducción asistida, y la falta de óvulos funcionales es una de las principales causas de infertilidad en mujeres mayores de 35 años.
Hasta ahora, las opciones se limitaban a donaciones de óvulos, lo que impedía a las mujeres o parejas obtener descendencia con su propio ADN.
El procedimiento del equipo estadounidense consiste en tomar el núcleo de una célula de piel y transferirlo a un óvulo donante al que se le ha extraído previamente su núcleo.
Para garantizar que el óvulo resultante tenga la mitad de cromosomas necesarios, los científicos desarrollaron un proceso llamado mitomeiosis, que permite a la célula dividirse sin duplicar el ADN, generando un óvulo con 23 cromosomas funcionales.
@awaytounderstand Como podemos fabricar un #ovulo a partir de #celulas de la #piel #ciencia #cienciaentiktok #datoscuriosos #datoscientificos #aprenderentiktok #onfertilidad #fertilidad
♬ sonido original – A Way to Understand
En el laboratorio, se produjeron 82 ovocitos funcionales, de los cuales un 9% llegó a desarrollarse hasta los seis días de cultivo, la etapa en que normalmente se transferiría al útero durante un tratamiento de fertilización in vitro.
Aún queda un largo camino para mejorar el método
Aunque el número de embriones viables fue limitado y algunos presentaron alteraciones cromosómicas, los investigadores consideran que se trata de una prueba de concepto prometedora.
Nuria Martí, primera autora del estudio, destacó que este enfoque podría, en el futuro, permitir que mujeres que carecen de ovocitos o parejas del mismo sexo tengan hijos con carga genética propia. Expertos como Ying Cheong, de la Universidad de Southampton, coinciden en que este hallazgo podría transformar la comprensión y el tratamiento de la infertilidad, aunque advierten que aún quedan al menos diez años de investigación antes de su aplicación clínica.
Este logro representa un paso más en la gametogénesis in vitro humana, consolidando el dominio de Mitalipov sobre la técnica SCNT y ofreciendo una esperanza real para quienes buscan alternativas a la reproducción asistida convencional.